
Кадровый состав сотрудников группы
Храпова Ксения Олеговна – к.х.н., с.н.с.
Тележкин Антон Алексеевич – к.х.н., с.н.с.
Сат Айыран Орланович – лаборант.
Направление (область) научных исследований и тематика лаборатории/группы
Базовым направлением работы группы служит создание оригинальной концепции использования функциональных ацетиленовых кетонов в качестве удобной и эффективной синтетической платформы для получения разнообразных, в том числе гетероатомных, функционализированных карбо- и гетероциклических систем. В основе методологии лежит применение в качестве структурной базы аминоацетиленовых кетонов, легко получаемых по реакции хемоселективного окислительного кросс-сочетания пропаргиламинов (синтезируемых по реакции аза-Фаворского из кетиминов и газообразного ацетилена) с цилкоалифатическими, ароматическими и гетероароматическими ацилхлоридами с использованием каталитической системы PdCl2/Ph3P/CuI/Et3N. Целью научно-исследовательской работы группы являются систематические исследования реакционной способности получаемых электронодефицитных ацетиленов в реакциях с различными, в том числе фосфорцентрированными, нуклеофилами.
Основные научные результаты (фундаментальные исследования)
1.Синтез аминоацетиленовых кетонов из пропаргиламинов и ацилхлоридов
В рамках научно-исследовательской работы группы был предложен оригинальный метод синтеза малоизученного класса электронодефицитных ацетиленов реакцией хемоселективного кросс-сочетания пропаргиламинов с ацилхлоридами в присутствии системы PdCl2/Ph3P/CuI/Et3N. Показано, что процесс успешно реализуется при небольшом нагревании (40–45 °C) в среде толуола в течение 2–3 ч хемоселективно с образованием соответствующих аминоацетиленовых кетонов с препаративным выходом 77–97%.
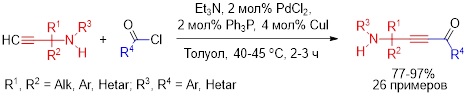
Неожиданным оказался факт инертности аминогруппы к реакции ацилирования как в условиях проведения процесса, так и при использовании трехкратного мольного избытка ацилхлорида.
Исходные пропаргиламины были получены оригинальной реакцией нуклеофильного присоединения газообразного ацетилена к кетиминам разнообразного строения с использованием суперосновной системы t-BuOK/ДМСО [Schmidt E.Yu., Bidusenko I.A., Protsuk N.I., Demyanov Y.V., Ushakov I.A., Trofimov B.A. Superbase-Promoted Addition of Acetylene Gas to the C=N Bond // Eur. J. Org. Chem. – 2019. – P. 5875–5881].
Volkov P.A., Khrapova K.O., Telezhkin A.A., Bidusenko I.A., Schmidt E.Yu., Albanov A.I., Trofimov B.A. Pd/Cu-Catalyzed Cross-Coupling of Densely Substituted Propargylamines with Aromatic Acyl Chlorides Followed by the Treatment with a Base: Access to Dihydro-3H-Pyrrol-3-Ones // Adv. Synth. Catal. – 2023. – V. 365. – P. 53–67. DOI: 10.1002/adsc.202201179.
2. Основно-каталитическая тандемная сборка 1,2-дигидро-3H-пиррол-3-онов из аминоацетиленовых кетонов
На основе оригинальной основно-каталитической реакции внутримолекулярной циклизации новой группы аминоацетиленовых кетонов разработана стратегия направленного синтеза 1,2-дигидро-3H-пиррол-3-онов – фармацевтически, синтетически и технически ценных и перспективных субстанций и строительных блоков. В качестве основных катализаторов были использованы KOH и Et2NH. Процесс реализуется в среде этанола при 40–55 °С в течение 8–17 ч, выходы целевых пирролонов достигают 92%.
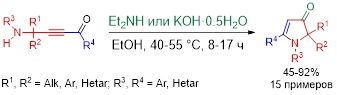
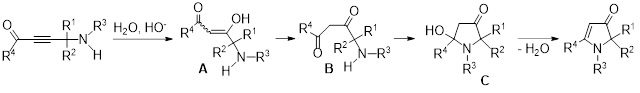
Схема тандемной сборки 1,2-дигидро-3H-пиррол-3-онов включает первоначальное присоединение молекулы воды в присутствии КОН с образованием енолов А, которые далее подвергаются перегруппировке в соответствующие 1,3-дикетоны В. Дальнейшая внутримолекулярная нуклеофильная атака аминогруппы по карбонильному фрагменту приводит к образованию промежуточных гидроксипирролидинонов C, которые после отщепления молекулы воды образуют целевые 1,2-дигидро-3H-пиррол-3-оны.
Volkov P.A., Khrapova K.O., Telezhkin A.A., Bidusenko I.A., Schmidt E.Yu., Albanov A.I., Trofimov B.A. Pd/Cu-Catalyzed Cross-Coupling of Densely Substituted Propargylamines with Aromatic Acyl Chlorides Followed by the Treatment with a Base: Access to Dihydro-3H-Pyrrol-3-Ones // Adv. Synth. Catal. – 2023. – V. 365. – P. 53–67. DOI: 10.1002/adsc.202201179.
3. Направленный синтез 1,2-дигидро-3H-пиррол-3-тионов на основе пропаргиламинов и ацилхлоридов
Открыта эффективная однореакторная стратегия синтеза 1,2-дигидро-3H-пиррол-3-тионов (практически неизвестных гетероциклических систем) на основе пропаргиламинов, ацилхлоридов и сульфида натрия. Целевая сборка включает первоначальное смешение пропаргиламина с ацилхлоридом в присутствии каталитической системы PdCl2/CuI/Ph3P (соотношение 2:4:2 моль%) в комбинированном растворителе Et3N/толуол при 40–45 °C в течение 3 ч с последующим добавлением к полученной реакционной смеси этанола и 2 эквивалентов Na2S∙9H2O и проведением процесса при 20–25 °С в течение 7 ч. Препаративный выход целевых функциональных гетероциклов достигает 91%.

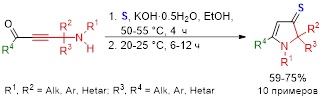
Показана принципиальная возможность применения в качестве стартового реагента элементной серы. Реакция включает первоначальное расщепление молекулы серы под действием гидроксида калия при 50–55 °С в течение 4 ч в растворе этанола и дальнейшее введение в реакционную смесь аминоацетиленового кетона. Выходы дигидро-3H-пиррол-3-тионов составляют 59–75%.
Разработан однореакторный подход к 1,2-дигидро-3Н-пиррол-3-селонам на основе пропаргиламинов, ацилхлоридов и элементного селена. Реакция включает открытое ранее получение аминоацетиленовых кетонов без препаративного выделения, к которым затем добавляется предварительно нагретая (70–75 °С, 5 ч) смесь Se/KOH (SnCl2)/EtOH с последующим перемешиванием при комнатной температуре в течение 10–11 ч.

Volkov P.A., Khrapova K.O., Vyi E.M., Telezhkin A.A., Bidusenko I.A., Albanov A.I., Schmidt E.Yu., Trofimov B.A. Dihydropyrrole-3-thiones: one-pot synthesis from propargylamines, acyl chlorides and sodium sulfide // Org. Biomol. Chem. – 2023. – V. 21. – P. 6903–6913. DOI: 10.1039/d3ob01061a.
Volkov P.A., Khrapova K.O., Vyi E.M., Telezhkin A.A., Bidusenko I.A., Albanov A.I., Shchepochkin A.V. Elemental sulfur as a trigger and reagent in cyclization of γ-aminoacetylenic ketones to 1,2-dihydro-3H-pyrrole-3-thiones // Mendeleev Commun. – 2025. – V. 35. – P. 102–104. DOI: 10.71267/mencom.7582.
Volkov P.A., Khrapova K.O., Telezhkin A.A., Vyi E.M., Trofimov A.B., Bidusenko I.A., Albanov A.I., Belogolova A.M., Trofimov B.A. One-pot three-component synthesis of stable pyrrole-3-selones using propargyl amines, acyl chlorides, and elemental selenium // Org. Biomol. Chem. – 2025. – V. 23. – P. 4702–4709. DOI: 10.1039/d5ob00200a.
4. Реакции вторичных фосфинхалькогенидов с аминоацетиленовыми кетонами
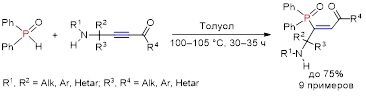
В рамках дальнейшего изучения синтетического потенциала аминоацетиленовых кетонов реализовано простое хемо-, регио- и стереоселективное присоединение дифенилфосфиноксида к аминоацетиленовым кетонам, 1,4-диорганил-(4-органиламино)алк-2-ин-1-онам, обеспечивающее эффективный синтез с выходом до 75% ранее неизвестной группы сложных полифункциональных молекул, Z-3-(дифенилфосфорил)-1,4-диорганил-4-(органиламино)алк-2-ен-1-онов, перспективных объектов для тонкого органического синтеза и фармакологических исследований. Реакция протекает при нагревании некаталитических условиях в среде толуола при 100–105 °С в течение 30–35 ч.
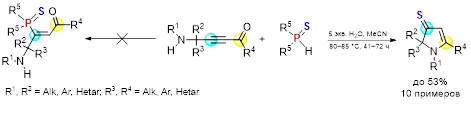
Обнаружен неожиданный факт переноса атома серы от молекулы вторичных фосфинсульфидов на тройную связь аминоацетиленовых кетонов, приводящего к синтезу 1,2-дигидро-3H-пиррол-3-тионов. Реакция реализуется в среде ацетонитрила при 80–85 °С в течение 41–72 ч с образованием целевых функциональных гетероциклических соединений с препаративным выходом до 53%. При этом продукты простого нуклеофильного присоединения вторичного фосфинсульфида к тройной связи электронодефицитного ацетилена образуются в следовых количествах.
Разработан удобный подход к стабильным замещенным 1,2-дигидро-3Н-пиррол-3-селонам, полученным в результате легкого переноса атома селена от вторичных фосфинселенидов к доступным аминоацетиленовым кетонам, синтезируемым оригинальным методом на основе пропаргиламинов и ацилхлоридов. Обнаруженная реакция открывает простой и прямой путь к новому семейству стабильных селонов, дополняющих, таким образом, ограниченный набор гетероциклов, содержащих двойные C=Se связи. Кардинальным отличием от известных ранее соединений является одновременное объединение в одной молекуле селоновой функции с жизненно важной пиррольной системой. Полученные данные способствуют лучшему пониманию электронной природы связи C=Se и закономерностей, определяющих ее стабильность.
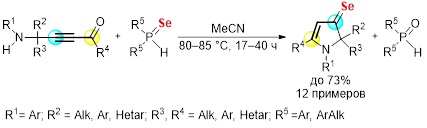
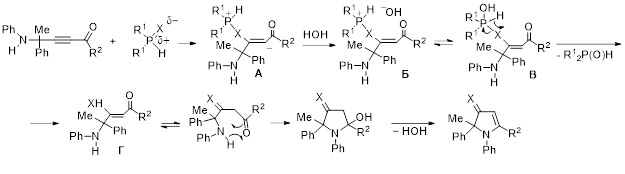
Схема образования 1,2-дигидро-3H-пиррол-3-тионов и -селонов, вероятно, включает нуклеофильное присоединение вторичного фосфинсульфида или фосфинселенида к тройной связи ацилацетилена (с участием атома халькогена, несущего частичный отрицательный заряд). Карбанионный центр образующегося при этом цвиттер-иона А нейтрализуется протоном воды, а возникающий гидроксид-анион атакует атом фосфора в катионе фосфония Б с образованием функционализированного фосфорана В. Одновременное расщепление связи фосфор-халькоген и формирование связи халькоген-водород приводит к образованию соответствующего вторичного фосфиноксида и винилтиола или винилселенола Г, который далее прототропно изомеризуется в соответствующий тион или селон. Внутримолекулярное нуклеофильное присоединение аминогруппы к карбонильной группе приводит к замыканию гидроксипирролидинового цикла. Отщепление молекулы воды с образованием двойной связи завершает процесс образования целевого пирролтиона или -селона.
Verkhoturova S.I., Volkov P.A., Bidusenko I.A., Arbuzova S.N., Zinchenko S.V., Trofimov B.A. Chemo-, regio-, and stereoselective catalyst-free addition of diphenylphosphine oxide to acetylenic amino ketones. Synthesis of Z-diphenylphosphoryl(organylamino)alkenones // Russ. Chem. Bull. – 2024. – Vol. 73. – No. 6. – P. 1738–1744. DOI: 10.1007/s11172-024-4291-x.
Volkov P.A., Verkhoturova S.V., Arbuzova S.N., Khrapova K.O., Bidusenko I.A., Zinchenko S.V., Trofimov B.A. Extraordinary sulfur/oxygen exchange between P=S and C=O bonds during the reaction of γ-aminoacetylenic ketones with secondary phosphine sulfides // Mendeleev Commun. – 2025. – V. 35. – P. 158–161. DOI: 10.71267/mencom.7627.
Volkov P., Verkhoturova S., Khrapova K., Arbuzova S., Bidusenko I., Albanov A., Trofimov B. Selenium transfer from secondary phosphine selenides to aminoacetylenic ketones: access to 1,2-dihydro-3H-pyrrole-3-selones with a stable C=Se bond // Org. Lett. – 2024. – V. 26. – N. 35. – P. 7336–7340. DOI: 10.1021/acs.orglett.4c02491.
5. Синтез и изучение нового класса соединений с устойчивыми связями C=Se – дигидропирролселонов на основе ацетилена, иминов и элементного селена
Показана принципиальная возможность получения нового класса гетероциклических соединений с устойчивыми C=Se связями, 1,2-дигидро-3Н-пиррол-3-селонов на основе аминоацетиленовых кетонов и элементного селена. Реакция включает первоначальную деструкцию элементного селена в присутствии системы КОН/этанол при 70-75 °С в течение 5 ч и последующее введение в полученную систему инона. Вторая стадия протекает в мягких условиях (20-25 °С, 7 ч) с образованием целевых гетероциклов с препаративным выходом 70-75%.
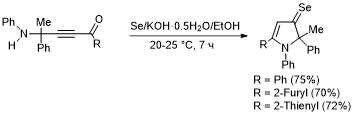
Найдены препаративные условия для синтеза 1,2-дигидро-3Н-пиррол-3-селонов в one-pot варианте из пропаргиламинов, ацилгалогенидов и элементного селена. Реакция включает предварительное приготовление двух реакционных смесей: расщепление элементного селена в присутствии системы Se/KOH/SnCl2/EtOH и окислительное кросс-сочетание пропаргиламинов с хлорангидридами карбоновых кислот с применением каталитической системы PdCl2/CuI/Ph3P/Et3N. Последующее их объединение и перемешивание при комнатной температуре в течение 10-11 ч завершает процесс. Выходы целевых продуктов достигают 75%.
Образование селонов начинается с реакции нуклеофильного присоединения гидроселенид-анионов (генерируемых в результате расщепления элементного селена под действием сильного основания или системы сильное основание/восстановитель) с образованием винилселенидов как интермедиатов. Последующая изомеризация приводит к соответствующим селонам. Внутримолекулярная циклизация аминогруппы с карбонильным фрагментом приводит к замыканию гидроксипирролов, дегидратация которых дает конечные пиррол-3-селоны.

Volkov P.A., Khrapova K.O., Telezhkin A.A., Vyi E.M., Trofimov A.B., Bidusenko I.A., Albanov A.I., Belogolova A.M., Trofimov B.A. One-pot three-component synthesis of stable pyrrole-3-selones using propargyl amines, acyl chlorides, and elemental selenium // Org. Biomol. Chem. – 2025. – V. 23. – P. 4702–4709. DOI: 10.1039/d5ob00200a
6. Некаталитическое региоспецифическое SNHAr фосфинилирование пиридинов Н-фосфинатами, инициируемое бензоилфенилацетиленом
Недавно [Trofimov B.A., Volkov P.A., Telezhkin A.A. Electron-Deficient Acetylenes as Three-Modal Adjuvants in SNH Reaction of Pyridinoids with Phosphorus Nucleophiles // Molecules. – 2021. – V. 26. – P. 6824. DOI: 10.3390/molecules26226824] нами был открыт новый тип SNHAr реакции азинов с фосфинхалькогенидами, новизна которого обусловлена использованием электронодефицитных ацетиленов в качестве триггеров/окислителей. Данную реакцию отличает также достаточно широкий субстратный охват азинов (пиридины, хинолины, изохинолины, акридины, фенантридины), фосфинхалькогенидов (оксиды, сульфиды, селениды) и электронодефицитных ацетиленов (алкилпропиолаты, терминальные и интернальные ацилацетилены, фенилцианоацетилен).
В продолжение этих исследований данная методология функционализации пиридиноидов была расширена на такой родственный вторичным фосфинхалькогенидам тип РН-нуклеофилов как эфиры Н-фосфиновых кислот. Эксперименты показали, что оптимальным для взаимодействия пиридина и его замещенных с производными Н-фосфинатов и бензоилфенилацетиленом является нагревание смеси до 50 °С без растворителя в течение 26–238 ч с образованием соответствующих 4-фосфинилпиридинов с препаративным выходом до 68%.

Механизм кросс-сочетания, вероятно, включает обратимое формирование 1,3(4)-диполя (интермедиат А) в результате нуклеофильной атаки атома азота пиридина на тройную связь ацилацетилена. Карбанионный центр интермедиата А нейтрализуется протоном фосфината с формированием промежуточной ионной пары Б. Однако, в отличие от аналогичной реакции с участием фосфинхалькогенидов, в реакционной смеси не было обнаружено ожидаемых N-бензоилэтенил-C-фосфинилированных дигидропиридинов В. Предположительно, вместо их формирования происходит окислительное элиминирование халкона от пиридиниевого катиона ионной пары Б. В этом случае бензоилэтенильный фрагмент, вероятно, отщепляется в виде аниона с одновременным отщеплением протона из положения 2 пиридинового кольца. В результате образуется новая ионная пара Г, которая далее путем 1,3-гидридного сдвига превращается в целевые продукты реакции.
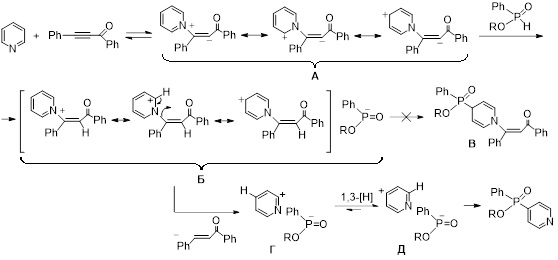
Механизм SNHAr реакции был уточнен на основе взаимодействия вторичных фосфинхалькогенидов и фосфинатов с пиридином-d5 и бензоилфенилацетиленом, а также с помощью квантовохимических расчетов.
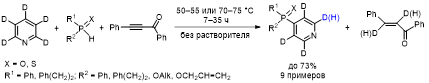
Во время реакции происходит H/D обмен в положении 2 пиридинового кольца. Такое возможно, если карбанионный центр цвиттер-иона А нейтрализуется дейтероном из положения 2 с образованием карбена Б. Последний присоединяет протон P-нуклеофила, формируя ионную пару В, которая далее через соответствующую катионную резонансную форму Г переходит в 4-фосфорилированный дигидропиридиновый интермедиат. Затем происходит 1,3-перенос дейтерия из положения 4 в положение 2, сопровождающийся миграцией двойной связи и приводящий к дигидропиридину Д. Данный интермедиат отщепляет халкон вместе с протием или дейтерием из положения 2, образуя замещенный пиридин.
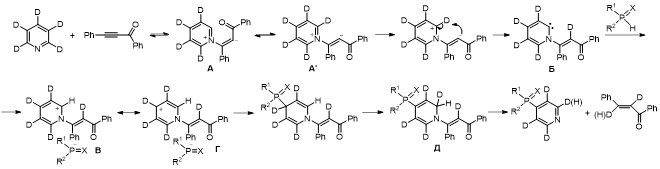
Khrapova K.O., Volkov P.A., Telezhkin A.A., Albanov A.I., Chupakhin O.N., Trofimov B.A. Catalyst- and solvent-free regiospecific SNHAr phosphinylation of pyridines with H-phosphinates mediated by benzoylphenylacetylene // Org. Biomol. Chem. – 2024. – V. 22. – N. 26. – P. 5419–5427. DOI: 10.1039/D4OB00661E.
Volkov P.A., Khrapova K.O., Telezhkin A.A., Albanov A.I., Yasnygin N.A., Trofimov A.B., Kuzmin A.V., Trofimov B.A. Catalyst-Free Nucleophilic Substitution of Deuterium in Pyridine‑d5 with Phosphorus Nucleophiles Triggered and Driven by Electrophilic Acetylenes: Mechanism Revisited // J. Org. Chem. – 2026. – V. 91. – P. 1422–1430. DOI: 10.1021/acs.joc.5c02728.
Гранты, контракты, хоздоговора, партнеры по инновационным исследованиям за последние 5 лет
РНФ 18-73-10080P ««Электрофильные ацетилены как триггеры и окислители в SNHAr-реакциях азинов с РН-нуклеофилами: развитие химии фосфорилированных азинов» (руководитель – к.х.н. П.А. Волков)
РНФ 25-23-00146 «Синтез и изучение нового класса соединений с устойчивыми связями C=Se – дигидропирролселонов на основе ацетилена, иминов и элементного селена» (руководитель – д.х.н. П.А. Волков)
Обзоры
Тележкин А.А., Волков П.А., Храпова К.О. Нуклеофильное замещение водорода в пиридине и его производных фосфорорганическими нуклеофилами в присутствии электронодефицитных ацетиленов // Журнал органической химии. – 2023. – Т. 59. – N 10. – С. 1269–1300. DOI: 10.31857/S0514749223100026.















