- Информация о материале
- Категория: Научные подразделения

Кадровый состав сотрудников группы
Храпова Ксения Олеговна – к.х.н., с.н.с.
Тележкин Антон Алексеевич – к.х.н., с.н.с.
Верхотурова Светлана Ильясовна – к.х.н., с.н.с.
Арбузова Светлана Николаевна – к.х.н., с.н.с.
Вый Екатерина Михайловна – лаборант.
Сат Айыран Орланович – лаборант.
Направление (область) научных исследований и тематика лаборатории/группы
Базовым направлением работы группы служит создание оригинальной концепции использования функциональных ацетиленовых кетонов в качестве удобной и эффективной синтетической платформы для получения разнообразных, в том числе гетероатомных, функционализированных карбо- и гетероциклических систем. В основе методологии лежит применение в качестве структурной базы аминоацетиленовых кетонов, легко получаемых по реакции хемоселективного окислительного кросс-сочетания пропаргиламинов (синтезируемых по реакции аза-Фаворского из кетиминов и газообразного ацетилена) с цилкоалифатическими, ароматическими и гетероароматическими ацилхлоридами с использованием каталитической системы PdCl2/Ph3P/CuI/Et3N. Целью научно-исследовательской работы группы являются систематические исследования реакционной способности получаемых электронодефицитных ацетиленов в реакциях с различными, в том числе фосфорцентрированными, нуклеофилами.
Основные научные результаты (фундаментальные исследования)
1.Синтез аминоацетиленовых кетонов из пропаргиламинов и ацилхлоридов
В рамках научно-исследовательской работы группы был предложен оригинальный метод синтеза малоизученного класса электронодефицитных ацетиленов реакцией хемоселективного кросс-сочетания пропаргиламинов с ацилхлоридами в присутствии системы PdCl2/Ph3P/CuI/Et3N. Показано, что процесс успешно реализуется при небольшом нагревании (40–45 °C) в среде толуола в течение 2–3 ч хемоселективно с образованием соответствующих аминоацетиленовых кетонов с препаративным выходом 77–97%.
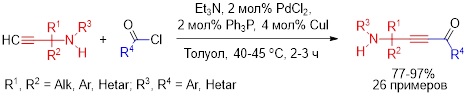
Неожиданным оказался факт инертности аминогруппы к реакции ацилирования как в условиях проведения процесса, так и при использовании трехкратного мольного избытка ацилхлорида.
Исходные пропаргиламины были получены оригинальной реакцией нуклеофильного присоединения газообразного ацетилена к кетиминам разнообразного строения с использованием суперосновной системы t-BuOK/ДМСО [Schmidt E.Yu., Bidusenko I.A., Protsuk N.I., Demyanov Y.V., Ushakov I.A., Trofimov B.A. Superbase-Promoted Addition of Acetylene Gas to the C=N Bond // Eur. J. Org. Chem. – 2019. – P. 5875–5881].
Volkov P.A., Khrapova K.O., Bidusenko I.A., Telezhkin A.A., Schmidt E.Yu., Albanov A.I., Trofimov B.A. Chemoselective cross-coupling of terminal propargylamines with (het)aroyl chlorides: synthesis of β-aminoacetylenic ketones bearing aromatic and heteroaromatic substituents // Russ. Chem. Bull. – 2022. – V. 71. – Р. 1514–1518. DOI: 10.1007/s11172-022-3558-3.
Volkov P.A., Khrapova K.O., Telezhkin A.A., Bidusenko I.A., Schmidt E.Yu., Albanov A.I., Trofimov B.A. Pd/Cu-Catalyzed Cross-Coupling of Densely Substituted Propargylamines with Aromatic Acyl Chlorides Followed by the Treatment with a Base: Access to Dihydro-3H-Pyrrol-3-Ones // Adv. Synth. Catal. – 2023. – V. 365. – P. 53–67. DOI: 10.1002/adsc.202201179.
2. Основно-каталитическая тандемная сборка 1,2-дигидро-3H-пиррол-3-онов из аминоацетиленовых кетонов
На основе оригинальной основно-каталитической реакции внутримолекулярной циклизации новой группы аминоацетиленовых кетонов разработана стратегия направленного синтеза 1,2-дигидро-3H-пиррол-3-онов – фармацевтически, синтетически и технически ценных и перспективных субстанций и строительных блоков. В качестве основных катализаторов были использованы KOH и Et2NH. Процесс реализуется в среде этанола при 40–55 °С в течение 8–17 ч, выходы целевых пирролонов достигают 92%.
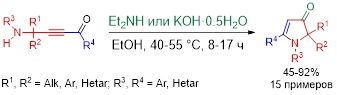
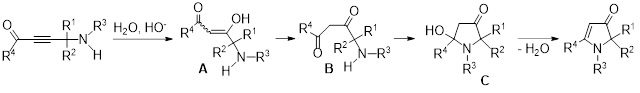
Схема тандемной сборки 1,2-дигидро-3H-пиррол-3-онов включает первоначальное присоединение молекулы воды в присутствии КОН с образованием енолов А, которые далее подвергаются перегруппировке в соответствующие 1,3-дикетоны В. Дальнейшая внутримолекулярная нуклеофильная атака аминогруппы по карбонильному фрагменту приводит к образованию промежуточных гидроксипирролидинонов C, которые после отщепления молекулы воды образуют целевые 1,2-дигидро-3H-пиррол-3-оны.
Volkov P.A., Khrapova K.O., Telezhkin A.A., Bidusenko I.A., Schmidt E.Yu., Albanov A.I., Trofimov B.A. Pd/Cu-Catalyzed Cross-Coupling of Densely Substituted Propargylamines with Aromatic Acyl Chlorides Followed by the Treatment with a Base: Access to Dihydro-3H-Pyrrol-3-Ones // Adv. Synth. Catal. – 2023. – V. 365. – P. 53–67. DOI: 10.1002/adsc.202201179.
3. Направленный синтез 1,2-дигидро-3H-пиррол-3-тионов на основе пропаргиламинов и ацилхлоридов
Открыта эффективная однореакторная стратегия синтеза 1,2-дигидро-3H-пиррол-3-тионов (практически неизвестных гетероциклических систем) на основе пропаргиламинов, ацилхлоридов и сульфида натрия. Целевая сборка включает первоначальное смешение пропаргиламина с ацилхлоридом в присутствии каталитической системы PdCl2/CuI/Ph3P (соотношение 2:4:2 моль%) в комбинированном растворителе Et3N/толуол при 40–45 °C в течение 3 ч с последующим добавлением к полученной реакционной смеси этанола и 2 эквивалентов Na2S∙9H2O и проведением процесса при 20–25 °С в течение 7 ч. Препаративный выход целевых функциональных гетероциклов достигает 91%.

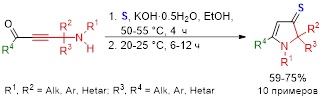
Показана принципиальная возможность применения в качестве стартового реагента элементной серы. Реакция включает первоначальное расщепление молекулы серы под действием гидроксида калия при 50–55 °С в течение 4 ч в растворе этанола и дальнейшее введение в реакционную смесь аминоацетиленового кетона. Выходы дигидро-3H-пиррол-3-тионов составляют 59–75%.
Volkov P.A., Khrapova K.O., Vyi E.M., Telezhkin A.A., Bidusenko I.A., Albanov A.I., Schmidt E.Yu., Trofimov B.A. Dihydropyrrole-3-thiones: one-pot synthesis from propargylamines, acyl chlorides and sodium sulfide // Org. Biomol. Chem. – 2023. – V. 21. – P. 6903–6913. DOI: 10.1039/d3ob01061a.
Volkov P.A., Khrapova K.O., Vyi E.M., Telezhkin A.A., Bidusenko I.A., Albanov A.I., Shchepochkin A.V. Elemental sulfur as a trigger and reagent in cyclization of γ-aminoacetylenic ketones to 1,2-dihydro-3H-pyrrole-3-thiones // Mendeleev Commun. – 2025. – V. 35. – P. 102–104. DOI: 10.71267/mencom.7582.
4. Реакции вторичных фосфинхалькогенидов с аминоацетиленовыми кетонами
В рамках дальнейшего изучения синтетического потенциала аминоацетиленовых кетонов реализовано простое хемо-, регио- и стереоселективное присоединение дифенилфосфиноксида к аминоацетиленовым кетонам, 1,4-диорганил-(4-органиламино)алк-2-ин-1-онам, обеспечивающее эффективный синтез с выходом до 75% ранее неизвестной группы сложных полифункциональных молекул, Z-3-(дифенилфосфорил)-1,4-диорганил-4-(органиламино)алк-2-ен-1-онов, перспективных объектов для тонкого органического синтеза и фармакологических исследований. Реакция протекает при нагревании некаталитических условиях в среде толуола при 100–105 °С в течение 30–35 ч.
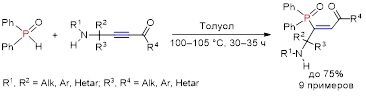
Обнаружен неожиданный факт переноса атома серы от молекулы вторичных фосфинсульфидов на тройную связь аминоацетиленовых кетонов, приводящего к синтезу 1,2-дигидро-3H-пиррол-3-тионов. Реакция реализуется в среде ацетонитрила при 80–85 °С в течение 41–72 ч с образованием целевых функциональных гетероциклических соединений с препаративным выходом до 53%. При этом продукты простого нуклеофильного присоединения вторичного фосфинсульфида к тройной связи электронодефицитного ацетилена образуются в следовых количествах.
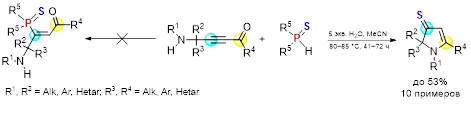
Разработан удобный подход к стабильным замещенным 1,2-дигидро-3Н-пиррол-3-селонам, полученным в результате легкого переноса атома селена от вторичных фосфинселенидов к доступным аминоацетиленовым кетонам, синтезируемым оригинальным методом на основе пропаргиламинов и ацилхлоридов. Обнаруженная реакция открывает простой и прямой путь к новому семейству стабильных селонов, дополняющих, таким образом, ограниченный набор гетероциклов, содержащих двойные C=Se связи. Кардинальным отличием от известных ранее соединений является одновременное объединение в одной молекуле селоновой функции с жизненно важной пиррольной системой. Полученные данные способствуют лучшему пониманию электронной природы связи C=Se и закономерностей, определяющих ее стабильность.
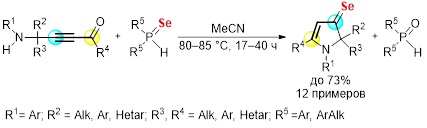
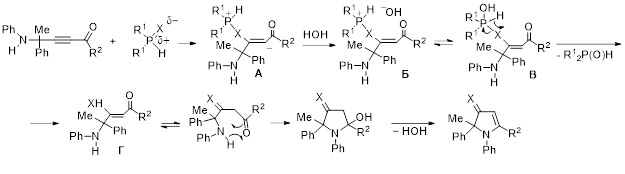
Схема образования 1,2-дигидро-3H-пиррол-3-тионов и -селонов, вероятно, включает нуклеофильное присоединение вторичного фосфинсульфида или фосфинселенида к тройной связи ацилацетилена (с участием атома халькогена, несущего частичный отрицательный заряд). Карбанионный центр образующегося при этом цвиттер-иона А нейтрализуется протоном воды, а возникающий гидроксид-анион атакует атом фосфора в катионе фосфония Б с образованием функционализированного фосфорана В. Одновременное расщепление связи фосфор-халькоген и формирование связи халькоген-водород приводит к образованию соответствующего вторичного фосфиноксида и винилтиола или винилселенола Г, который далее прототропно изомеризуется в соответствующий тион или селон. Внутримолекулярное нуклеофильное присоединение аминогруппы к карбонильной группе приводит к замыканию гидроксипирролидинового цикла. Отщепление молекулы воды с образованием двойной связи завершает процесс образования целевого пирролтиона или -селона.
Verkhoturova S.I., Volkov P.A., Bidusenko I.A., Arbuzova S.N., Zinchenko S.V., Trofimov B.A. Chemo-, regio-, and stereoselective catalyst-free addition of diphenylphosphine oxide to acetylenic amino ketones. Synthesis of Z-diphenylphosphoryl(organylamino)alkenones // Russ. Chem. Bull. – 2024. – Vol. 73. – No. 6. – P. 1738–1744. DOI: 10.1007/s11172-024-4291-x.
Volkov P.A., Verkhoturova S.V., Arbuzova S.N., Khrapova K.O., Bidusenko I.A., Zinchenko S.V., Trofimov B.A. Extraordinary sulfur/oxygen exchange between P=S and C=O bonds during the reaction of γ-aminoacetylenic ketones with secondary phosphine sulfides // Mendeleev Commun. – 2025. – V. 35. – P. 158–161. DOI: 10.71267/mencom.7627.
Volkov P., Verkhoturova S., Khrapova K., Arbuzova S., Bidusenko I., Albanov A., Trofimov B. Selenium transfer from secondary phosphine selenides to aminoacetylenic ketones: access to 1,2-dihydro-3H-pyrrole-3-selones with a stable C=Se bond // Org. Lett. – 2024. – V. 26. – N. 35. – P. 7336–7340. DOI: 10.1021/acs.orglett.4c02491.
5. Некаталитическое региоспецифическое SNHAr фосфинилирование пиридинов Н-фосфинатами, инициируемое бензоилфенилацетиленом
Недавно [Trofimov B.A., Volkov P.A., Telezhkin A.A. Electron-Deficient Acetylenes as Three-Modal Adjuvants in SNH Reaction of Pyridinoids with Phosphorus Nucleophiles // Molecules. – 2021. – V. 26. – P. 6824. DOI: 10.3390/molecules26226824] нами был открыт новый тип SNHAr реакции азинов с фосфинхалькогенидами, новизна которого обусловлена использованием электронодефицитных ацетиленов в качестве триггеров/окислителей. Данную реакцию отличает также достаточно широкий субстратный охват азинов (пиридины, хинолины, изохинолины, акридины, фенантридины), фосфинхалькогенидов (оксиды, сульфиды, селениды) и электронодефицитных ацетиленов (алкилпропиолаты, терминальные и интернальные ацилацетилены, фенилцианоацетилен).
В продолжение этих исследований данная методология функционализации пиридиноидов была расширена на такой родственный вторичным фосфинхалькогенидам тип РН-нуклеофилов как эфиры Н-фосфиновых кислот. Эксперименты показали, что оптимальным для взаимодействия пиридина и его замещенных с производными Н-фосфинатов и бензоилфенилацетиленом является нагревание смеси до 50 °С без растворителя в течение 26–238 ч с образованием соответствующих 4-фосфинилпиридинов с препаративным выходом до 68%.

Механизм кросс-сочетания, вероятно, включает обратимое формирование 1,3(4)-диполя (интермедиат А) в результате нуклеофильной атаки атома азота пиридина на тройную связь ацилацетилена. Карбанионный центр интермедиата А нейтрализуется протоном фосфината с формированием промежуточной ионной пары Б. Однако, в отличие от аналогичной реакции с участием фосфинхалькогенидов, в реакционной смеси не было обнаружено ожидаемых N-бензоилэтенил-C-фосфинилированных дигидропиридинов В. Предположительно, вместо их формирования происходит окислительное элиминирование халкона от пиридиниевого катиона ионной пары Б. В этом случае бензоилэтенильный фрагмент, вероятно, отщепляется в виде аниона с одновременным отщеплением протона из положения 2 пиридинового кольца. В результате образуется новая ионная пара Г, которая далее путем 1,3-гидридного сдвига превращается в целевые продукты реакции.
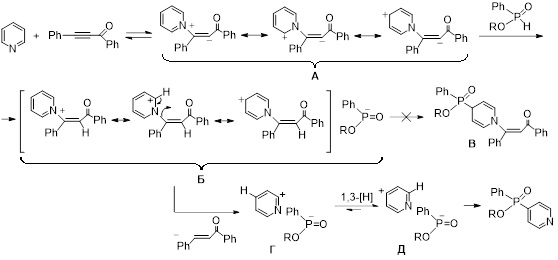
Khrapova K.O., Volkov P.A., Telezhkin A.A., Albanov A.I., Chupakhin O.N., Trofimov B.A., Catalyst- and solvent-free regiospecific SNHAr phosphinylation of pyridines with H-phosphinates mediated by benzoylphenylacetylene // Org. Biomol. Chem. – 2024. – V. 22. – N. 26. – P. 5419–5427. DOI: 10.1039/D4OB00661E.
6. Окислительное кросс-сочетание вторичных фосфинхалькогенидов с аминоспиртами и аминофенолами
Были получены новые данные по изучению реакций окислительного кросс-сочетания вторичных фосфинхалькогенидов с таким новым типом реагентов, как аминоспирты и аминофенолы. Исследования показали, что реакция с участием аминоспиртов протекает в мягких условиях (20–25 °С, 2–4 ч) в присутствии системы CCl4/Et3N с хемоселективным образованием амидов халькогенофосфиновых кислот с выходом 70–84%.
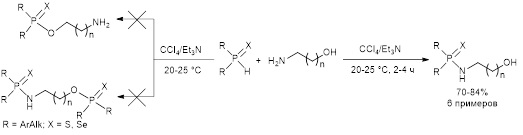
В противоположность аминоспиртам аминофенолы в аналогичных условиях реагируют с вторичными фосфинхалькогенидами с образованием исключительно эфиров халькогенофосфиновых кислот с препаративным выходом 70–84%.
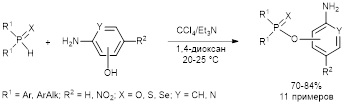

Khrapova K.O., Telezhkin A.A., Volkov P.A., Larina L.I., Pavlov D.V., Gusarova N.K., Trofimov B.A. Oxidative cross-coupling of secondary phosphine chalcogenides with amino alcohols and aminophenols: aspects of the reaction chemoselectivity // Org. Biomol. Chem. – 2021. – V. 19. – P. 5098–5107. DOI: 10.1039/d1ob00287b.
Гранты, контракты, хоздоговора, партнеры по инновационным исследованиям за последние 5 лет
MK-5606.2021.1.3 победитель “Конкурса 2021 года на право получения грантов Президента Российской Федерации для государственной поддержки молодых российских ученых – кандидатов наук” к.х.н. Храпова Ксения Олеговна
РНФ 18-73-10080P ««Электрофильные ацетилены как триггеры и окислители в SNHAr-реакциях азинов с РН-нуклеофилами: развитие химии фосфорилированных азинов» (руководитель – к.х.н. П.А. Волков)
РНФ 25-23-00146 «Синтез и изучение нового класса соединений с устойчивыми связями C=Se – дигидропирролселонов на основе ацетилена, иминов и элементного селена» (руководитель – д.х.н. П.А. Волков)
Обзоры
Trofimov B.A., Volkov P.A., Telezhkin A.A. Electron-Deficient Acetylenes as Three-Modal Adjuvants in SNH Reaction of Pyridinoids with Phosphorus Nucleophiles // Molecules. – 2021. – V. 26. – P. 6824. DOI: 10.3390/molecules26226824.
Тележкин А.А., Волков П.А., Храпова К.О. Нуклеофильное замещение водорода в пиридине и его производных фосфорорганическими нуклеофилами в присутствии электронодефицитных ацетиленов // Журнал органической химии. – 2023. – Т. 59. – N 10. – С. 1269–1300. DOI: 10.31857/S0514749223100026.
- Информация о материале
- Категория: Научные подразделения

Кадровый состав
В группе работают 6 человек, из них 1 доктор наук, 2 кандидата наук и 1 аспирант:
Трофимов Александр Борисович – ведущий научный сотрудник, д.х.н., профессор РАН.
Скитневская Анна Дмитриевна – ведущий научный сотрудник, к.х.н.
Белоголова Александра Максимовна – научный сотрудник, к.х.н.
Ясныгин Никита Александрович – аспирантГришкова Валерия Михайловна – инженер.
Меринов Иван Александрович – лаборант.
Основное направление исследований
Квантовохимическое изучение строения, свойств и реакционной способности соединений, являющихся конечными и исходными продуктами, а также итермедиатами синтезов на базе ацетилена. Теоретическое изучение гетероароматических и гетероциклических молекул, обладающих установленной или потенциальной биологической активностью, а также представляющих собой блоки или прототипы более сложных биологических систем в их основном, возбужденных и ионных состояниях. Исследование связанных с возбужденными состояниями процессов молекулярной и ионизационной динамики, а также межмолекулярного переноса заряда и энергии. Развитие перспективных для решения перечисленных задач методов расчета электронной структуры на основе теории пропагаторов.
Основные научные результаты
1.Развитие пропагаторных методов расчета электронной структуры
Расчет электронной структуры молекул и атомов лежит в основе квантовохимической методологии и обеспечивает успех всех стадий теоретического моделирования. В то время как методы расчета электронной структуры основного состояния на сегодня хорошо разработаны, изучение возбужденных и ионных состояний до сих пор представляет собой серьезную проблему, в первую очередь, из-за отсутствия эффективных и универсальных расчетных схем, способных надежно описывать сложные реорганизационные процессы в электронной оболочке при переходах между состояниями. Чрезвычайно полезным в этом отношении оказался класс методов на основе теории пропагаторов (функций Грина), которые могут быть получены в рамках приближения алгебраического диаграммного построения (ADC) и т. н. формализма промежуточных состояний (ISR).
Сотрудники группы квантовой химии внесли свой вклад в создание методов ADC/ISR и продолжают активно участвовать в их развитии совместно с коллегами из Гейдельбергского университета (Германия). В частности, было разработано семейство методов IP/EA-ADC/ISR для изучения свойств молекул в стабильных и метастабильных состояниях, образующихся в результате отрыва и присоединения электрона, создано соответствующее программное обеспечение, связанное с пакетами программ Gamess и Q-Chem, а также исследована точность новых методов. В серии недавних работ на примере спектров ионизации g-пирона и 6,6-диметилфульвена было установлено важное преимущество расчетных схем IP-ADC(3) по отношению к конкурирующим методам IP-EOM-CCSD, состоящее в способности схем IP-ADC(3) всегда достаточно адекватно описывать ионизационные сателлиты и качественно правильно передавать их роль в фотоэлектронных спектрах.
L. Dempwolff, A. C. Paul, A. M. Belogolova, A. B. Trofimov, A. Dreuw, Intermediate state representation approach to physical properties of molecular electron-detached states. I. Theory and implementation // J. Chem. Phys.- 2020.- Vol. 152.- P. 024113/1-16. [doi: 10.1063/1.5137792]
L. Dempwolff, A. C. Paul, A. M. Belogolova, A. B. Trofimov, A. Dreuw, Intermediate state representation approach to physical properties of molecular electron-detached states. II. Benchmarking // J. Chem. Phys.- 2020.- Vol. 152.- P. 024125/1-12. [doi: 10.1063/1.5137794]
L. Dempwolff, A. M. Belogolova, A. B. Trofimov, A. Dreuw, Intermediate state representation approach to physical properties of molecular electron-attached states: Theory, implementation, and benchmarking // J. Chem. Phys.- 2021.- Vol. 154.- P. 104117/1-16. [doi: 10.1063/5.0043337]
L. Dempwolff, A. M. Belogolova, T. Sommerfeld, A. B. Trofimov, A. Dreuw, CAP/EA-ADC Method for Metastable Anions: Computational Aspects and Application to Resonances of Norbornadiene and 1,4-Cyclohexadiene // J. Chem. Phys.- 2021.- Vol. 155.- P. 054103/1-13. [https://doi.org/10.1063/5.0057737]
А.Б. Трофимов, Э.К. Якимова, Е.В. Громов, А.Д. Скитневская, Теоретическое исследование электронного строения и спектра ионизации γ-пирона // ЖОрХ.- 2023.- Т. 59, № 10.- С. 1363-1374. [DOI: 10.31857/S0514749223100075]
A.B. Trofimov, A.D. Skitnevskaya, A.M. Belogolova, E.K. Iakimova, E.V. Gromov, A study of the ionization spectrum of 6,6-dimethylfulvene using algebraic-diagrammatic construction and coupled cluster methods // Russian Journal of Physical Chemistry A.- 2024.- Vol. 98, No. 5.- P. 878-885. [https://doi.org/10.1134/S0036024424050297]
3.Теоретическое изучение флуорофоров
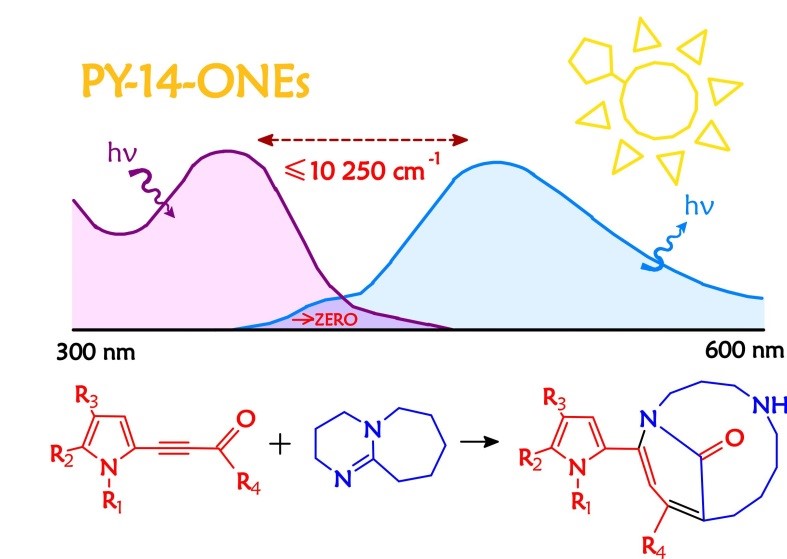
Получаемые в результате реакций ацетилена гетероароматические соединения нередко оказываются представителями новых классов флуорофоров или функционализрованными членами уже известных семейств флуорофоров. Квантовохимические расчеты позволяют успешно интерпретировать проявляемые этими соединениями свойства. Прежде всего это касается наблюдаемых спектров поглощения и испускания. Кроме того, при помощи расчетов часто могут быть объяснены различные закономерности, например, связанные с влиянием заместителя и растворителя, а также необычные или неожиданные особенности фотохимии и фотофизики. Так, в недавней работе в результате проведенного квантовохимического исследования удалось объяснить гигантские сдвиги Стокса (от 8000 до 10250 обратных сантиметров), которые демонстрируют молекулы из открытого в лаборатории нового класса флуорофоров PY-14-ONEs на основе пирролилдиазабицикло [8.3.1] тетрадекадиенонов, являющихся 14-членными гетероциклами с дополнительным мостиком. Легкое получение путем необычной реакции расширения цикла DBU и практически нулевое перекрывание полос поглощения и испускания вследствие больших стоксовских сдвигов делают флуорофоры PY-14-ONEs перспективными для многих приложений. Другим примером теоретических исследований в данной области являются флуорофоры из семейства BODPY, получаемые на основе ранее разработанного в лаборатории синтеза на базе функционализированных пирролов, получаемых из ацетилена и оксимов кетонов.
S.A. Tikhonov, E.V. Fedorenko, A.G. Mirochnik, I.S. Osmushko, A.D. Skitnevskaya, A.B. Trofimov, V.I. Vovna, Spectroscopic and quantum chemical study of difluoroboron β-diketonate luminophores: Isomeric acetylnaphtholate chelates // Spectrochim. Acta A.- 2019.- Vol. 214.- P. 67-78. [https://doi.org/10.1016/j.saa.2019.02.002]
S.A. Tikhonov, A.E. Sidorin, A.A. Ksenofontov, D.Yu. Kosyanov, I.S. Samoilov, A.D. Skitnevskaya, A.B. Trofimov, E.V. Antina, M.B. Berezin, V.I. Vovna, XPS and quantum chemical analysis of 4Me-BODIPY derivatives // Phys. Chem. Chem. Phys.- 2023.- Vol. 25.- P. 5211-5225. [https://doi.org/10.1039/D2CP04541A]
B.A. Trofimov, L.N. Sobenina, O.V. Petrova, E.F. Sagitova, K.B. Petrushenko, D.N. Tomilin, E.G. Martyanova, V.F. Razumov, L.A. Oparina, I.A. Ushakov, D.V. Korchagin, A.M. Belogolova, A.B. Trofimov, Macrocyclic bridgehead fluorophores, pyrrolyl-diazabicyclo[8.3.1]tetradecadienones, with giant Stokes shifts // J. Org. Chem.- 2024.- Vol. 89, Iss. 24.- P. 18142-18158. [https://doi.org/10.1021/acs.joc.4c02002]
3. Исследования процессов межмолекулярного переноса заряда и энергии в высоковозбужденых молекулярных системах
Понимание механизмов взаимодействия ионизирующего излучения с веществом, в частности, процессов перераспределения энергии и заряда после образования высоковозбужденных катион-радикалов с вакансиями внутривалентных уровней важно для разработки стратегий защиты биологических объектов от радиации, развития лучевой терапии, а также создания радиационно устойчивых материалов. Особенностью обсуждаемых высоковозбужденных состояний является их склонность к автоионизации, то есть релаксации за счет выброса электрона, в результате которого обычно образуется двукратно-заряженный катион в основном состоянии и свободный электрон, уносящий выделившуюся энергию. В системах с межмолекулярными связями автоионизация может иметь локальный и нелокальный характер. В первом случае электрон выбрасывается той же молекулой, которая была изначально ионизирована, что соответствует хорошо известному Оже-распаду. Во втором случае происходит ионизация соседней молекулы, что соответствует менее изученным процессам межмолекулярного кулоновского распада (ICD) или распада посредством переноса электрона (ETMD).
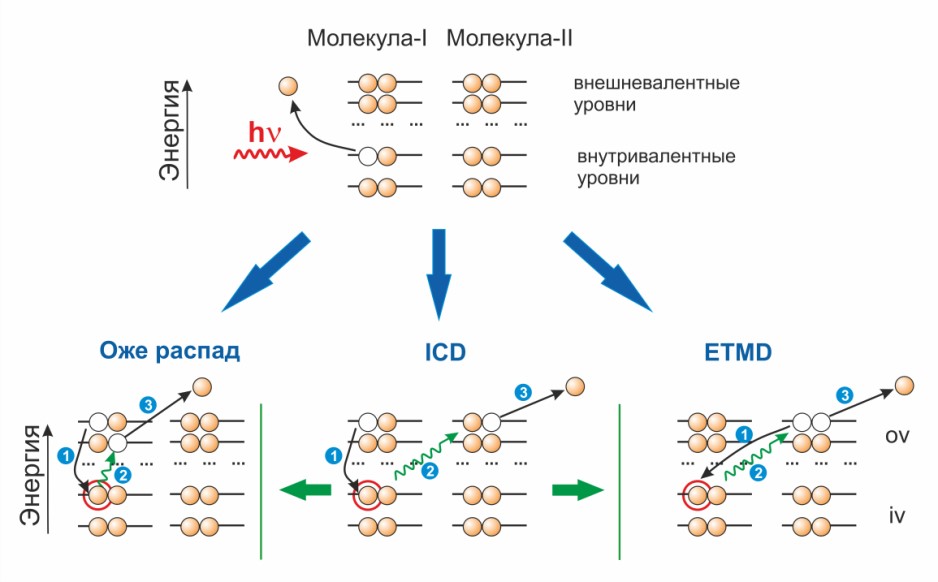
Результаты последних исследований однозначно указывают на то, что нелокальные релаксационные процессы доминируют в живой природе, где биологически активные молекулы находятся в водном или белковом окружении, а также могут быть связаны друг с другом межмолекулярными связями (ДНК). Осознание данных фактов в сочетании с бурным развитием экспериментальной базы привело в последние годы к существенному росту интереса к исследованиям ICD и сходных процессов. При этом особая роль отводится квантовохимическим расчетам, поскольку здесь интерпретация и планирование эксперимента невозможны без привлечения адекватного теоретического моделирования. Однако, особенность рассматриваемых состояний диктует необходимость применения нестандартных квантовохимических подходов, таких как пропагаторные методы.
Наличие в активе нашей группы таких расчетных схем и опыта работы с ними позволяют нам успешно работать в данном направлении. В частности, благодаря нашим теоретическим результатам стали возможны исследования, в которых впервые явным образом было показано, что ICD возможен в гидратированных биомолекулах, а также в димерах органических молекул. В другой важной работе с нашим участием, посвященной ICD в газофазных димерах ароматических молекул, удалось впервые однозначно определить предпочтительные взаимные ориентации входящих мономеров, что указывает на возможность создания на этой базе принципиально нового чувствительного метода изучения строения вещества. Еще одним заметным вкладом в изучение межмолекулярных релаксационных процессов является работа, в которой было доказано, что сверхбыстрый межмолекулярный перенос протона может успешно конкурировать с автоионизацией.
Ren, E. Wang, A.D. Skitnevskaya, A.B. Trofimov, K. Gokhberg, A. Dorn, Experimental evidence for ultrafast intermolecular relaxation processes in hydrated biomolecules // Nature Physics.- 2018.- Vol. 14.- P. 1062-1066. [https://doi.org/10.1038/s41567-018-0214-9]
Zhou, S. Jia, A.D. Skitnevskaya, E. Wang, T. Hähnel, E.K. Grigoricheva, X. Xue, J.-X. Li, A.I. Kuleff, A. Dorn, X. Ren, Concerted double hydrogen-bond dreaking by intermolecular coulombic decay in the formic acid dimer // J. Phys. Chem. Lett. - 2022.- Vol. 13, N. 19.- P. 4272-4279. [https://doi.org/10.1021/acs.jpclett.2c00957]
Zhou, S. Jia, X. Xue, A.D. Skitnevskaya, E. Wang, X. Wang, X. Hao, Q. Zeng, A.I. Kuleff, A. Dorn, X. Ren, Revealing the role of N heteroatoms in noncovalent aromatic interactions by ultrafast intermolecular coulombic decay // J. Phys. Chem. Lett.- 2024.- Vol. 15, N. 5.- P. 1529-1538. [https://doi.org/10.1021/acs.jpclett.3c02979]
A.D. Skitnevskaya, K. Gokhberg, A.B. Trofimov, E.K. Grigoricheva, A.I. Kuleff, L.S. Cederbaum, Two-sided impact of water on the relaxation of inner-valence vacancies of biologically relevant molecules // J. Phys. Chem. Lett.- 2023.- Vol. 14.- P. 1418-1426. [https://doi.org/10.1021/acs.jpclett.2c03654]
Gao, A. D. Skitnevskaya, E. Wang, H. Yuan, X. Ren, H. Lin, Z. Yan, S. Zhang, S. Gu, B. Yang, F. Fang, S. Yan, D. Guo, X. Zhu, D. Zhao, C. Shao, Z. Huang, X. Xue, X. Hao, J. Zhou, T. Zhang, J. Li, X. Yan, M. Wang, L. Mao, D. Yin, M. Tang, Y. Yuan, J. Yang, A.B. Trofimov, L.S. Cederbaum, A.I. Kuleff, X. Ma, S. Xu, Damaging intermolecular relaxation processes initiated by heavy-ion irradiation of hydrated biomolecules // Phys. Rev. X.- 2025.- Vol. 15.- P. 11053/1-17. [https://doi.org/10.1103/PhysRevX.15.011053]
Гранты
Грант РНФ 23-23-00485 «Исследование эволюции электронных состояний с вакансиями внутренних уровней в гидратированных биомолекулах» (руководитель к.х.н. А.Д. Скитневская)
Грант РФФИ 19-03-00947 «Теоретическое изучение эволюции и каналов распада высоковозбужденных состояний гидратированных гетероциклических молекул – структурных фрагментов биосистем» (руководитель к.х.н. А.Д. Скитневская)
Грант РФФИ 19-33-90213 «Расчеты спектров ионизации молекул, содержащих тяжелые атомы, методами электронного пропагатора с учетом релятивистских эффектов» (руководитель к.х.н. А.М. Белоголова)
Защиты диссертаций
А.М. Белоголова, "Методы электронного пропагатора для изучения молекулярных состояний, образующихся при отрыве и присоединении электрона" диссертация на соискание ученой степени кандидата химических наук по специальности 1.4.4. "Физическая химия", 15 сентября 2021 г. (диссертационный совет 24.2.306.04 при Иркутском государственном университете).
- Информация о материале
- Категория: Научные подразделения
кандидат географических наук Заведующий лабораторией 8 (3952) 45-31-68
Емельянова Наталия Владимировна
Страница в разработке...
- Информация о материале
- Категория: Научные подразделения

Кадровый состав
В группе работают 2 человека, из них 1 доктор наук, 1 кандидат наук:
Паршина Лидия Никифоровна – ведущий научный сотрудник, д.х.н.
Грищенко Людмила Анатольевна – старший научный сотрудник, к.х.н.
Направление научных исследований
Разработка методов функционализации полисахаридов и других биоактивных молекул с целью получения фармацевтически и промышленно важных продуктов – перспективных биологически активных субстанций и наностабилизирующих матриц. В основу исследований положены реакции алкинил-производных полисахаридов, синтез которых, разработанный нами на примере пропаргилирования арабиногалактана, отличается мягкими условиями и высокими выходами целевых продуктов.
Введение в биообъекты ацетиленовых групп открывает большие возможности для их функционализации путем классических и современных (с использованием металлокомплексного катализа) реакций терминальных ацетиленов: нуклеофильного присоединения, ацетилен-алленовой изомеризации, азид-алкинового циклоприсоединения, кросс-сочетания, аминометилирования и др.
Ещё одним направлением исследования является систематическое изучение реакции комплексообразования N-функционализированных имидазольных лигандов: N-алкенил-, N-алкинилимидазолов и -бензимидазолов, разработка удобных подходов к синтезу новых металлокомплексов - потенциальных биологически активных веществ и перспективных прекурсоров лекарственных препаратов, проявляющих по данным фармакологов высокую противогипоксическую, противовоспалительную, противоболевую и ранозаживляющую активность.
Основные научные результаты за 2020 - 2024 гг.

1.Развитие методологии катализируемого золотом гидроаминирования пропаргиловых эфиров арабиногалактана жизненно важными азотистыми гетероциклами.
Разработан метод синтеза фармакологически перспективных имидазол- и бензимидазолпроизводных арабиногалактана (АГ) с выходом до 97 % (степень замещения до 1.8) по реакции катализируемого Au(III) нуклеофильного присоединения азотистых гетероциклов к пропаргиловым эфирам арабиногалактана. Установлено, что в условиях гидроаминирования Au(III) восстанавливается с образованием главным образом Au(0) и небольшого количества соединения Au(I) золота, которые присутствуют в составе имидазолпроизводных АГ в виде частиц размером 190-640 нм. Гидрохлориды полученных золотосодержащих имидазолпроизводных арабиногалактана показывают высокую бактериостатическую активность в отношении тестовых грамм-положительных (Enterococcus durans and Bacillus subtilis) микроорганизмов, таким образом, подтверждая свои перспективы как новые биоактивные агенты на основе арабиногалактана.
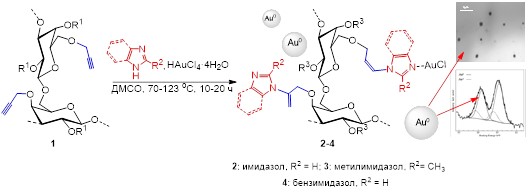
Grishchenko L. A., Parshina L. N., Larina L. I., Belovezhetz L. A., Klimenkov I. V., Ustinov A. Yu., Trofimov B. A. Arabinogalactan propargyl ethers: Au-catalysed hydroamination by imidazols // Carbohydrate Polymers. – 2020. – V. 246. – Article number 116638. DOI: 10.1016/j.carbpol.2020.116638.
2.Палладий-катализируемое кросс-сочетание пропаргиловых эфиров арабиногалактана с 5-бромсалициловой кислотой.
Реакцией кросс-сочетания пропаргиловых эфиров АГ с солями 5-бромсалициловой кислоты с выходом до 90% синтезированы ранее неизвестные салицилаты АГ – перспективные хелатирующие лиганды, объекты для медицины и фармакологии. Реакция протекает в ДМСО при 70-95 оС в присутствии каталитических систем Pd(Ph3P)4/PPh3 с CuBr (CuI) и пиперидина или 1,8-диазабицикло-[5.4.0]ундец-7-ена (ДБУ) как основания. Степень замещения арабиногалактана пропинилсалицилатными фрагментами достигает 1.0 и 0.7 в реакциях с пиперидином и ДБУ, соответственно. В случае пиперидина наряду с основным процессом наблюдается ранее неизвестное (для реакции Соногашира) гидроаминирование пропаргильных групп с последующим гидролизом образующихся енаминов.
Полученные салицилатпроизводные арабиногалактана в отличие от исходного АГ, его пропаргиловых эфиров и солей салициловой кислоты демонстрируют высокую антикоагулянтную активность, характеризующуюся увеличением показателя активированного частичного тромбопластинового времени (AЧТВ).
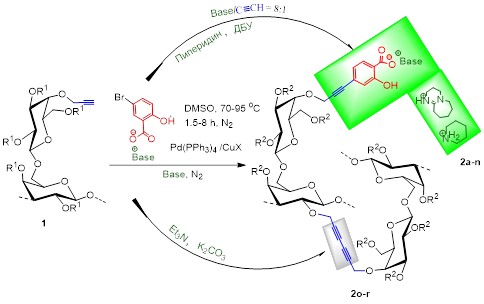
Grishchenko L. A., Parshina L. N., Larina L. I., Kostyro Ya. A., Trofimov B. A. Pd-catalyzed cross-coupling of arabinogalactan propargyl ethers with 5-bromosalicylic acid // Carbohydrate Polymers. – 2021. – V. 273. – Article number 118561. https://doi.org/10.1016/j.carbpol.2021.118561
3. A3- кросс-сочетание пропаргилированного арабиногалактана с альдегидами и вторичными циклическими аиминам
Синтезировано семейство новых фармакологически перспективных аминометилпропаргилпроизводных арабиногалактана реакцией CuI-катализируемого A3-сочетания (ДМСО, 23-65 оС) пропаргиловых эфиров полисахарида с альдегидами и вторичными циклическими аминами. Были получены производные арабиногалактана, содержащие фенил-, пиридин-, фурановые заместители в комбинации с пиперидин-, пирролидин-, морфолиновыми фрагментами, с выходом вплоть до 95% и степенью замещения от 0.3 до 2.0. Некаталитический вариант аминоалкилирования (96-100 оС, степень замещения до 1.1) протекает как по этинил, так и по гидроксильным центрам макромолекулы, приводя к продуктам преимущественно С-замещения.
Некоторые из синтезированных соединений и продуктов их гидрохлорирования показывают высокую бактериостатическую активность в отношении грамм-отрицательных микроорганизмов.
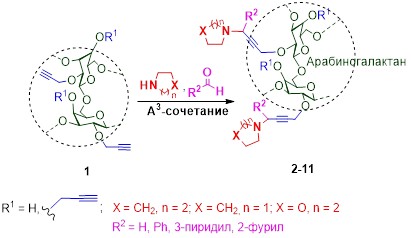
Grishchenko L. A., Parshina L. N., Larina L. I., Belovezhetz L. A., Trofimov B. A. Arabinogalactan propargyl ethers in the A3-coupling reaction with aldehydes and secondary cyclic amines // Carbohydrate Polymers. – 2023. – V. 300. – Article number 120239. https://doi.org/10.1016/j.carbpol.2022.120239.
II. Виниловые эфиры целлюлозы
Различные мерсеризованные целлюлозы (порошкообразная и сульфатная целлюлоза) успешно провинилированы ацетиленом в водном растворе гидроксидов щелочных металлов (KOH или NaOH) при 125-140 оС. В зависимости от условий реакции степень замещения (СЗ) гидроксильных групп высокореакционноспособными полимеризующимися винилоксигруппами составила 0.08-0.73, выход винилцеллюлозы 24-75%. Процесс сопровождается щелочной деструкцией макромолекулы целлюлозы.
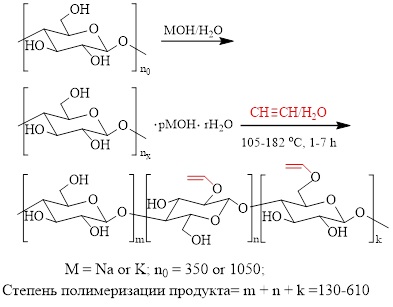
Parshina L. N., Oparina L. A., Tantsyrev A. P., Gusarova N. K., Trofimov B. A. NaOH(KOH)-catalyzed vinylation of cellulose with acetylene gas in water // Cellulose. – 2020. – V. 27, no. 16. P.9271-9283. DOI: 10.1007/s10570-020-03435-9.
III. Металлокомплексы N-алкенил- и N-алкинилимидазолов
Металлокомплексы N-алкенил- и N-алкинилимидазолов были синтезированы прямым взаимодействием компонентов – лигандов и солей металлов в органических растворителях.
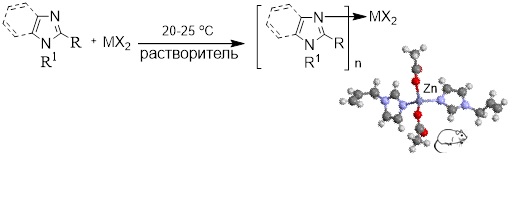
R = H, Me;
R1 = CH=CH2, CH2CH=CH2, CH2C≡CH, CH=CHPh, C(CH3)=CH2;
M = Zn(II), Co(II), Cu(II), Ni(II); n = 2, 4; X = Cl, OAc, gfac;
Растворитель = ацетон, этанол,
Полученные металлокомплексы исследовались в ряде медицинских учреждений, таких как Первый Московский государственный медицинский университет им. И. М. Сеченова, Кубанский государственный медицинский университет, Ростовский государственный медицинский университет и др. Помимо установленной ранее высокой противогипоксической активности комплексов ацетата цинка с N-винил- и N-аллилимидазолами обнаружена высокая ранозаживляющая активность цинковых комплексов N-аллил- и N-изопропенилимидазолов. Кроме того, комплекс ацетата цинка с N-изопропенилимидазолом проявил высокую эффективность в качестве противовоспалительного, антиоксидантного, антимикробного и минерализующего средства при лечении экспериментального парадонтоза крыс.
Свистунов А. А., Тарасов В. В., Лебедева С. А., Козин С. В., Мельник С. И., Недорубов А. А., Чубарев В. Н., Курынина К. О., Трофимов Б. А., Паршина Л. Н. Комплексные соединения цинка с N-аллилимидазолом как ранозаживляющие средства // Патент РФ № 2719360 (приоритет от 04.10.2019, зарегистр. 17.04.2020, заявка № 2019131333), Бюл. Изобр. 2020, № 11.
Свистунов А. А., Тарасов В. В., Лебедева С. А., Козин С. В., Мельник С. И., Недорубов А. А., Чубарев В. Н., Курынина К. О., Трофимов Б. А., Паршина Л. Н. Комплексное соединение цинка с N-изопропенилимидазолом как ранозаживляющее средство // Патент РФ № 2725634 (приоритет от 04.10.2019, зарегистр. 03.07.2020, заявка № 2019131335), Бюл. Изобр. 2020, № 19.
Smirnov V. I., Sinegovskaya L. M., Parshina L. N., Artem’ev A. V, Sterkhova I. V. Copper(ii), cobalt(ii),manganese(ii) and nickel(ii) bis(hexafluoroacetylacetonate) complexes with N-vinylimidazole // Mendeleev Commun. 2020. V. 30, no. 2. P. 246-248.
Sterkhova I. V., Parshina L. N., Grishchenko L. A., Borodina T. N., Belovezhets L. A., Semenov V. A. Metal complexes propargyl imidazoles with zinc (II) and cobalt (II) chlorides: synthesis, structure and properties // Международная конференция по химии «Байкальские чтения-2023». Тезисы докл. Иркутск, 2023. С. 147.
Sterkhova I. V., Parshina L. N., Grishchenko L. A., Borodina T. N., Belovezhets L. A. Semenov V. A. Complexes of zinc(II) chloride and acetate with propargylimidazoles: synthesis, structure and non-covalent interactions // Structural Chemistry. – 2023. – V. 34. – Iss. 6. – P. 2249-2262. РНФ-23-23-10007, https://doi.org/10.1007/s11224-023-02245-6
Sterkhova I. V., Parshina L. N., Grishchenko L. A., Borodina T. N., Belovezhets L. A. Semenov V. A. Synthesis, Structure, and Antimicrobial Properties of New Cobalt(II) Complexes with 1-Propargylimidazoles // Current Organic Chemistry. – 2024. – V. 28. – Iss. 9. – P. 708-715. РНФ-23-23-10007, IF 2.37 Q3 DOI: https://doi.org/10.2174/0113852728295396240314054651.
Sterkhova I. V., Parshina L. N., Grishchenko L. A., Borodina T. N., Belovezhets L. A. Semenov V. A. Six-coordinated complexes of Co(II), Ni(II) and Cu(II) chlorides with N-propargylimidazoles: Synthesis, structure, antimicrobial activity, AIM analysis and molecular docking Polyhedron. – 2024. – V. 260. – 117093 (c. 1-11). РНФ-23-23-10007, IF 2.52(2023), 2.68?(2024) Q2?, AQ3? https://doi.org/10.1016/j.poly.2024.117093
Чернигова П. О., Синеговская Л. М., Паршина Л. Н., Стерхова И. В., Смирнов В. И. Координационные комплексы бис-гексафторацетилацетонатов меди (II), кобальта (II) с N-стирилбензимидазолом. // Известия ВУЗов. Прикладная химия и биотехнология. – 2024 – Т. 14. – N 2. – С. 157-165. DOI: 10.21285/achb.913. No IF/
Sterkhova I. V., Parshina L. N., Grishchenko L. A., Borodina T. N., Belovezhets L. A. Semenov V. A. Role of Noncovalent Interactions in Structure and Properties of New Metal Complexes with N-Substituted Imidazoles // Book of abstracts 3 rd International Symposium “Noncovalent Interactions in Synthesis, Catalysis, and Crystal Engineering” NCI-2024. Тезисы докл. Новосибирск,19-25 August, 2024. С. 51.
Sterkhova I. V., Parshina L. N., Grishchenko L. A., Borodina T. N., Belovezhets L. A. Semenov V. A. Metal Complexes of Cobalt Chloride with Vinyl-, Allyl- and Styrylbenzimidazole Ligands: Synthesis, Structure, and Properties // ChemistrySelect. – 2024. – V. 9. – Iss. 36. – e202403393 (c. 1-14). РНФ-23-23-10007, IF 2.23, Q2, DOI: https://doi.org/10.1002/slct.202403393
Galenko-Yaroshevsky P. A., Pavlyuchenko I. I., Shelemekh O. V., Trofimov B. A., Parshina L. N., Popkov V. L., Demyanenko S. A., Tsymbalov O. V., Zadorozhniy A. V, Zelenskaya A. V., Nektarevskaya I. B., Sergeeva A. V., Korovaykin N. E., Lebedeva S. A. Study of anti-inflammatory, antioxidant, antimicrobial and mineralizing effects of an N-isopropenylimidazole zinc metal complex derivative in experimental endodontic-periodontal lesions in rats // Research Results in Pharmacology. – 2024. – V. 10. – Iss. 4. – P. 1–13. https://doi.org/10.18413/rrpharmacology.10.515 Q3.
- Информация о материале
- Категория: Научные подразделения
Подробная информация о работе коллектива
Информационно-просветительские ресурсы
 |
 |




















